
关于本中心开展医疗器械拓展性临床试验的信息公示
由北京佰仁医疗科技股份有限公司发起“评价Renato™介入式瓣中瓣系统有效性和安全性的多中心临床试验”(方案编号BRYL2020A),在首都医科大学附属北京安贞医院心脏瓣膜外科中心开展,主要研究者为张海波主任,试验于2021年04月23日通过医院伦理委员会批准,2021年05月28日在科室召开启动会,至2022年03月25日完成10例入组,截止2022年08月25日,受试者正常随访且身体状况良好。自2022年04月全国入组结束后,研究者在本中心日常临床诊疗过程中,仍然发现“此前植(介)入的人工生物心脏瓣膜已经发生损毁需要接受治疗,且面临常规外科手术换瓣较高风险”急需治疗的患者,因“介入式瓣中瓣器械”在国内无同类上市产品。为满足公众临床需要,使临床急需治疗的患者能够尽快获得救治。研究者与申办方、临床试验机构、伦理委员会多次沟通后,认为“Renato™介入式瓣中瓣系统”适用于国家药监局、国家卫生健康委发布的《医疗器械拓展性临床试验管理规定(试行)》,且本中心研究者已通过实施上述临床试验积累较多手术经验,目前临床有急需要治疗的患者,综上所述决定在本中心开展拓展性临床试验。
“评价Renato™介入式瓣中瓣系统有效性和安全性的拓展性临床试验”,于2022年09月29日获得本中心伦理批件,2023年02月23日签署试验协议,2023年02月24日在申办者所在地北京市药品监督管理局进行备案。现根据国家有关要求,将开展拓展性临床试验有关信息予以公示(详见附件1、2),并承诺将严格按照国家《医疗器械拓展性临床试验管理规定(试行)》及本中心管理制度要求,开展本次拓展性临床试验。
首都医科大学附属北京安贞医院
药物临床试验机构
2023年5月10日
附件1:拓展性临床试验方案摘要
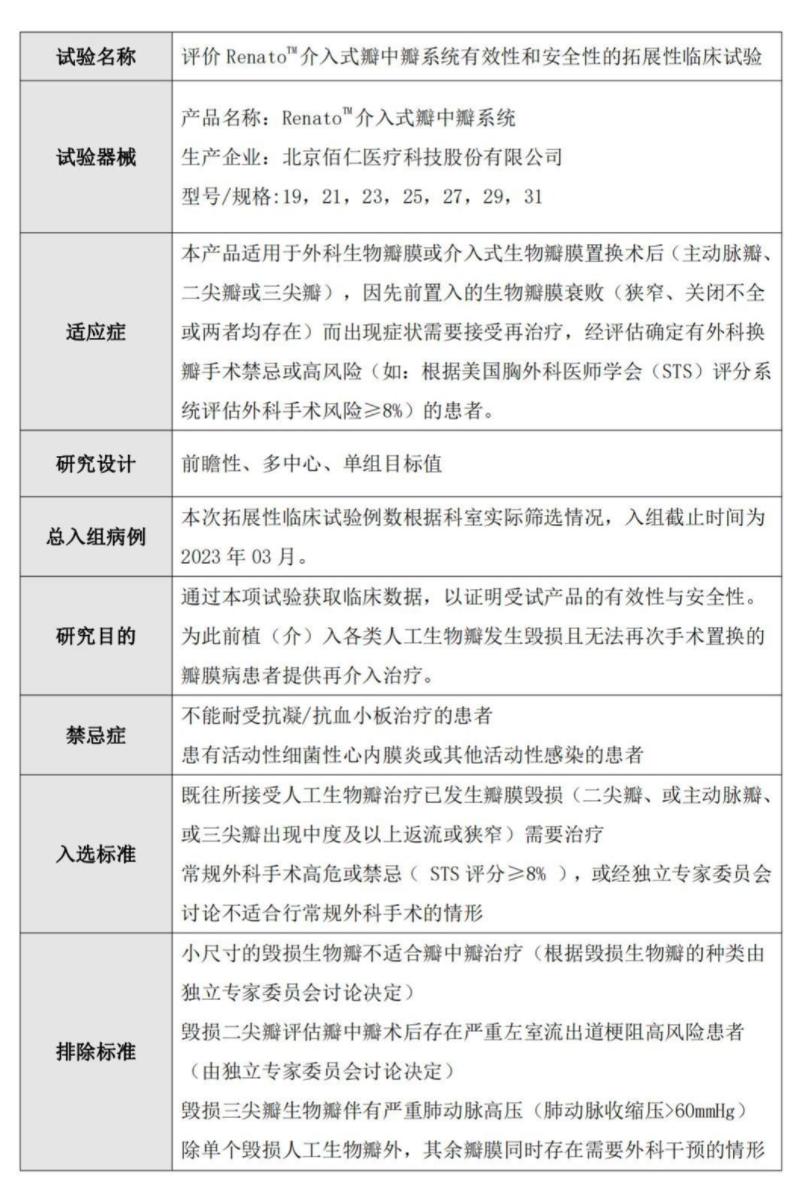
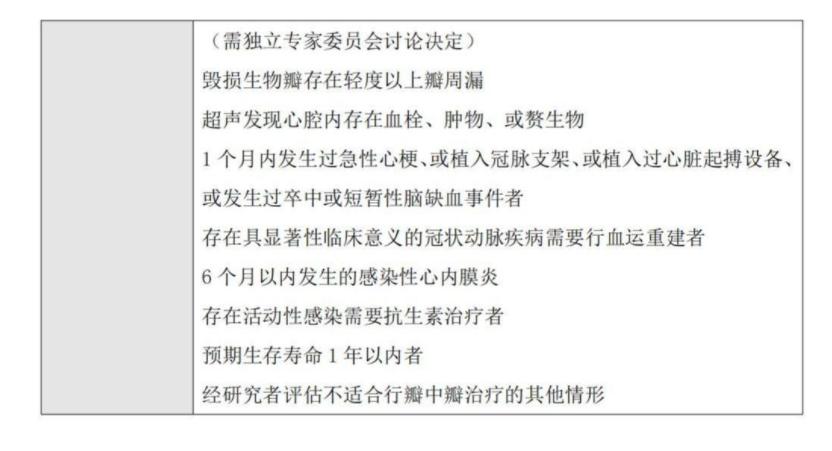
附件2:本中心伦理批件
上一篇: 医务处重要通知
下一篇: 临床生物样本资源中心试剂耗材遴选




















